Sviluppo di complessi metallici per applicazioni in diagnostica e terapia
Lo scopo di questa linea di ricerca è quello di sviluppare complessi metallici per imaging diagnostico multimodale e agenti teranostici, cioè composti in grado di combinare in un’unica molecola proprietà terapeutiche e di imaging. In particolare, si prepareranno precursori di Ru e Re adatti ad essere coniugati con agenti per terapia fotodinamica (PDT), cioè fotosensibilizzatori che – quando irradiati con luce visibile – generano ROS (reactive oxygen species).
Per esempio, un coniugato Ru-porfirina potrebbe combinare la fototossicità e l’affinità per i tessuti tumorali della porfirina con la citotossicità del frammento metallico portando ad effetti additivi; inoltre, l’emissione della porfirina può essere sfruttata per determinare la biodistribuzione dell’addotto a livello cellulare tramite microscopia di fluorescenza.
La coniugazione con Re/99mTc porterebbe a coppie di composti congeneri (matched pairs): il coniugato non-radioattivo di Re utilizzabile per la caratterizzazione chimica, imaging di fluorescenza e PDT, e quello di 99mTc – emettitore-gamma – potenzialmente adatto per imaging bimodale (fluorescenza e SPECT). Un esempio schematico del cosiddetto matched-pair approach è riportato nella seguente figura. maggiori dettagli su questo approccio si possono trovare nella nostra recente pubblicazione "Towards matched pairs of porphyrin-Re(I)/99mTc(I) conjugates that combine photodynamic activity with fluorescence- and radio-imaging." ChemMedChem 2014, 9, 1231–1237.DOI: 10.1002/cmdc.201300501.
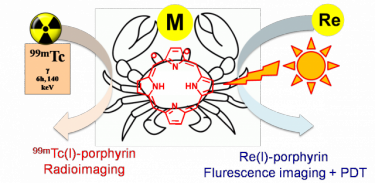
Quindi, più specificamente, verranno sviluppati precursori di Ru e Re adatti per essere coniugati con porfirine che rechino siti di legame periferici (da mono- a tridentati), cioè complessi che abbiano un opportuno numero di siti di coordinazione disponibili per la coniugazione e leganti ancillari altamente idrofilici per favorire la solubilità in acqua.
Il risultato più rilevante ottenuto nel corso della mia carriera nel settore della Medicinal Inorganic Chemistry è stato sicuramente l'aver sviluppato il NAMI-A, un composto di coordinazione di Ru(III) dotato di notevole attività antimetastatica che è ben noto nella comunità dei chimici bioinorganici come uno degli esempi di composti antitumorali inorganici non-platino (lo si trova anche nei libri di testo di Chimica Inorganica, si veda ad esempio la quinta edizione del ben noto Inorganic Chemistry, autori Shriver & Atkins). La formula del NAMI-A e un'immagine di un macro-campione del composto sono riportate di seguito.
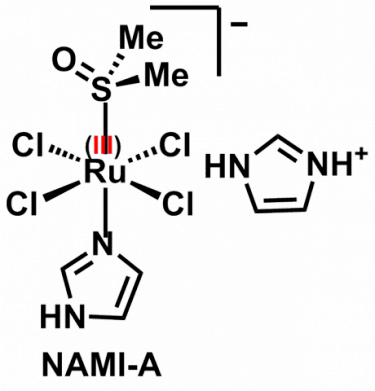
Il ruolo pionieristico svolto dal mio gruppo - insieme a pochissimi altri - nel settore dei composti antitumorali di rutenio è ben illustrato dal seguente grafico, che riporta il numero di pubblicazioni su questo argomento dal 1990 al 2011.
Quando, alla fine degli anni '80, iniziai la mia ricerca sui composti di rutenio come antitumorali, c'erano al massimo altri due o tre gruppi al mondo che lavoravano su questo argomento. All'epoca, tutto l'intersse era rivolto sui composti antitumorali di platino. In virtù delle eccellenti proprietà antimetastatiche dimostrate su modelli di tumori animali, nel 1999 il NAMI-A fu il primo complesso di Ru al mondo ad essere introdotto in fase clinica 1, cioè ad essere saggiato sull'uomo. Da allora (vedi grafico sopra), il numero di pubblicazioni sui composti antitumorali di rutenio è cresciuto con andamento quasi esponenziale. Dal 2008 al 2011 il NAMI-A, in combinazione con la gemcitabina, è stato somministrato a 32 pazienti affetti da carcinoma polmonare a cellule non-piccole in uno studio di fase clinica 1-2 presso il Netherland Cancer Institute di Amsterdam. I risultati di questo studio clinico sono in fase di pubblicazione:"Phase I/II study with ruthenium compound NAMI-A and gemcitabine in patients with non-small cell lung cancer after first line therapy." Invest. New Drugs .... DOI: 10.1007/s10637-014-0179-1.
Una caratteristica distintiva del NAMI-A, che lo rende diverso dalla maggior parte dei composti antitumorali, è la sua modesta tossicità in vitro verso linee cellulari di tumori solidi. Molto recentemente si è ottenuto al riguardo un risultato del tutto inatteso: il NAMI-A è infatti risultato essere altamente citotossico nei confronti di linee cellulari di leucemia (si veda Dalton Trans. 2014, 43, 12150 – 12155. DOI: 10.1039/C4DT01356E.). Questa scoperta potrebbe aprire nuovi scenari per l'utilizzo del complesso nell'uomo.
Il mio ruolo nel settore della medicinal inorganic chemistry è ben riconosciuto all'interno della comunità scientifica dei chimici bioinorganici. Ho partecipato attivamente a tutte le Azioni COST in questo campo a partire dal 1997 ( COST Chemistry Action D1), svolgendo anche il ruolo di vice-Chairman (2000-2003) e quindi di Chairman (2003-2006) della COST Chemistry Action D20 ‘Metal compounds in the treatment of cancer and viral diseases’. Nel 2011 sono stato l'editore, per i tipi della Wiley-VCH, del libro intitolato Bioinorganic Medicinal Chemistry (ISBN 978-3-527-32631-0) che raccoglie contributi da parte dei più prestigiosi scienziati del settore.
Pubblicazioni pertinenti dal 2009
1) T. Gianferrara, I. Bratsos, E. Alessio*
A Categorization of Metal Anticancer Compounds Based on Their Mode of Action.
Dalton Trans., 2009, 7588-7598. Perspective Article
2) T. Gianferrara, I. Bratsos, E. Iengo, B. Milani, A. Oštrić, C. Spagnul, E. Zangrando, E. Alessio*
Synthetic strategies towards ruthenium-porphyrin conjugates for anticancer activity.
Dalton Trans., 2009, 10742-10756.
3) T. Gianferrara, A. Bergamo, I. Bratsos, B. Milani, C. Spagnul, G. Sava, E. Alessio
Ruthenium-porphyrin conjugates with cytotoxic and phototoxic antitumor activity.
J. Med. Chem., 2010, 53, 4678-4690.
4) I. Bratsos, T. Gianferrara, E. Alessio,* C. G. Hartinger, M. A. Jakupec, B. K. Keppler
Ruthenium and Other Non-platinum Anticancer Compounds.
in Bioinorganic Medicinal Chemistry, E. Alessio ed., Wiley-VCH, Weinheim, 2011, pp. 151-174.
5) I. Bratsos,* D. Urankar, E. Zangrando, P. Genova-Kalou, J. Košmrlj, E. Alessio, I. Turel*
1-(2-picolyl)-substituted 1,2,3-triazole as novel chelating ligand for the preparation of ruthenium complexes with potential anticancer activity.
Dalton Trans. 2011, 40, 5188 – 5199.
6) I. Bratsos,* C. Simonin, E. Zangrando, T. Gianferrara, A. Bergamo, E. Alessio*
New half sandwich-type Ru(II) coordination compounds characterized by the fac-Ru(dmso-S)3 fragment: influence of the face-capping group on the chemical behavior and in vitro anticancer activity.
Dalton Trans. 2011, 40, 9533 – 9543.
7) I. Bratsos,* E. Mitri, F. Ravalico, E. Zangrando, T. Gianferrara, A. Bergamo, E. Alessio*
New half sandwich Ru(II) coordination compounds for anticancer activity
Dalton Trans. 2012, 41, 7358 – 7371.
8) A. Rilak, I. Bratsos,* E. Zangrando, J. Kljun,I. Turel, Ž. D. BugarÄić, E. Alessio*
Factors that influence the antiproliferative activity of half sandwich RuII-[9]aneS3coordination compounds: activation kinetics and interaction with guanine derivatives.
Dalton Trans. 2012, 41, 11608 – 11618.
9) G. Ragazzon, I. Bratsos, E. Alessio,* L. Salassa,*A. Habtemariam, R. McQuitty, G. J. Clarkson, P. J. Sadler*
Design of Photoactivatable Metallodrugs: Selective and Rapid Light-induced Ligand Dissociation from Half-Sandwich [Ru([9]aneS 3 )(N–N')(py)]2+ Complexes.
Inorg. Chim. Acta 2012, 393, 230-238.
10) C. Spagnul, R. Alberto,* G. Gasser, S. Ferrari, V. Pierroz, A. Bergamo, T. Gianferrara,* E. Alessio
Novel water-soluble 99mTc(I)/Re(I)-porphyrin conjugates as potential multimodal agents for molecular imaging.
J. Inorg. Biochem. 2013, 122, 57–65.
11) I. Finazzi, I. Bratsos, T. Gianferrara, A. Bergamo, N. Demitri, G. Balducci, E. Alessio*
Photolabile RuII Half-Sandwich Complexes Suitable for Developing “Caged†Compounds: Chemical Investigation and Unexpected Dinuclear Species with Bridging Diamine Ligands.
Eur. J. Inorg. Chem. 2013, 4743–4753. DOI:10.1002/ejic.201300792
12) J. Kljun,I. Bratsos, E. Alessio, G. Psomas, U. Repnik, M. Butinar, B. Turk, I. Turel*
New Uses for Old Drugs: Attempts to Convert Quinolone Antibacterials into Potential Anticancer Agents Containing Ruthenium.
Inorg. Chem. 2013, 52, 9039–9052. DOI: 10.1021/ic401220x
13) T. Gianferrara, C. Spagnul,R. Alberto,* G. Gasser,S. Ferrari, V. Pierroz, A. Bergamo, E. Alessio*
Towards matched pairs of porphyrin-Re(I)/99mTc(I) conjugates that combine photodynamic activity with fluorescence- and radio-imaging.
ChemMedChem 2014, 9, 1231–1237.DOI: 10.1002/cmdc.201300501.
14) A. Rilak, I. Bratsos,* E. Zangrando, J. Kljun, I. Turel, ZÌŒ. D. BugarcÌŒicÌ, E. Alessio*
New Water-Soluble Ruthenium(II) Terpyridine Complexes for Anticancer Activity: Synthesis, Characterization, Activation Kinetics, and Interaction with Guanine Derivatives.
Inorg. Chem. 2014, 53, 6113–6126. DOI 10.1021/ic5005215.
15) S. Pillozzi, L. Gasparoli, M. Stefanini, M. D’Amico, M. Ristori, E. Alessio, F. Scaletti, A. Becchetti, A. Arcangeli*, L. Messori*
NAMI-A is Highly Cytotoxic Toward Leukaemia Cell Lines: Evidence of Inhibition of KCa3.1 Channels.
Dalton Trans. 2014, 43, 12150 – 12155. DOI:10.1039/C4DT01356E.
Gruppo di ricerca
| Gruppo Prof. Alessio |